DINH DƯỠNG VÀ CẤU TRÚC GIẤC NGỦ ĐỐI VỚI SUY GIẢM NHẬN THỨC
CƠ CHẾ TÁC ĐỘNG KÉP CỦA DINH DƯỠNG VÀ CẤU TRÚC GIẤC NGỦ ĐỐI VỚI SUY GIẢM NHẬN THỨC: MỘT PHÂN TÍCH TỔNG QUAN HỆ THỐNG
1. Đặt vấn đề
Trong bối cảnh già hóa dân số, suy giảm nhận thức nhẹ (MCI) và bệnh Alzheimer đang trở thành gánh nặng y tế công cộng. Báo cáo của Ủy ban Lancet (2020) xác định rằng 40% các trường hợp sa sút trí tuệ có thể ngăn ngừa hoặc trì hoãn thông qua việc quản lý các yếu tố nguy cơ lối sống. Mặc dù dinh dưỡng và giấc ngủ thường được nghiên cứu riêng biệt, các bằng chứng sinh học thần kinh hiện đại gợi ý một mối liên hệ biện chứng chặt chẽ giữa trục chuyển hóa và cơ chế phục hồi thần kinh. Bài viết này nhằm mục đích tổng hợp, so sánh và trừu tượng hóa các cơ chế tác động của hai biến số này dựa trên dữ liệu định lượng mới nhất.
2. Vai trò của Dinh dưỡng: Từ chuyển hóa đến bảo vệ thần kinh
Các nghiên cứu dịch tễ học đã chuyển dịch từ quan điểm "vi chất đơn lẻ" sang "mô hình ăn uống tổng thể". Nổi bật là nghiên cứu dọc của Morris và cộng sự (2015) trên tạp chí Alzheimer's & Dementia. Sử dụng mô hình hồi quy tuyến tính hỗn hợp, kết quả cho thấy những cá nhân tuân thủ nghiêm ngặt chế độ ăn MIND (Mediterranean-DASH Intervention for Neurodegenerative Delay) có tốc độ suy giảm nhận thức chậm hơn đáng kể (, ), tương đương với não bộ trẻ hơn 7.5 tuổi.
Cơ chế sinh học được khái quát hóa qua hai con đường chính:
- Giảm stress oxy hóa: Các thực phẩm giàu Vitamin E và flavonoid (rau lá xanh, quả mọng) trung hòa các gốc tự do, bảo vệ màng tế bào thần kinh.
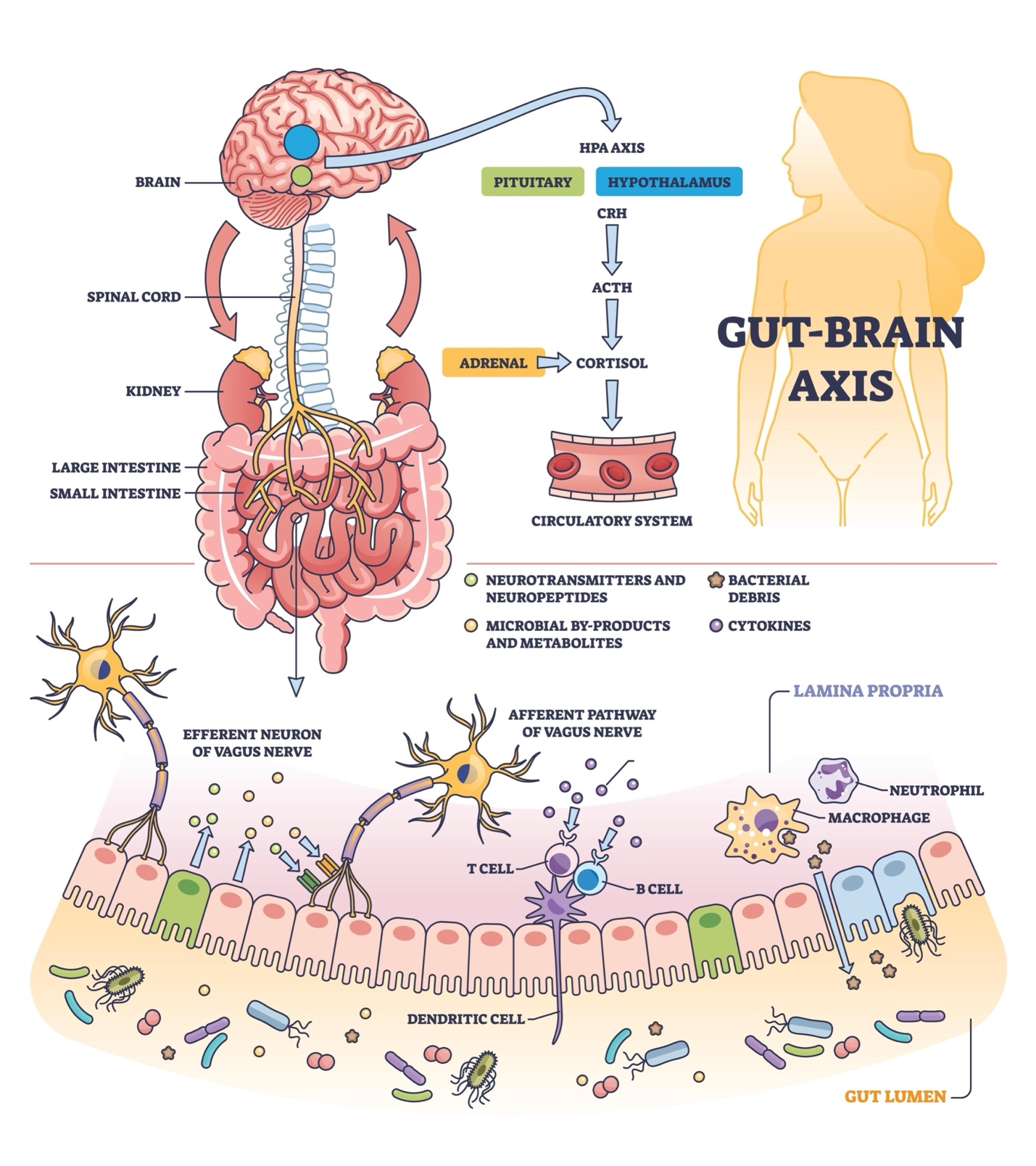
- Trục Ruột - Não (Gut-Brain Axis): Chế độ ăn giàu chất xơ và ít chất béo bão hòa nuôi dưỡng hệ vi sinh vật đường ruột lành mạnh, ức chế sự sản sinh các cytokine gây viêm (như IL-6, TNF-) có khả năng vượt qua hàng rào máu não và gây viêm thần kinh.
3. Cấu trúc Giấc ngủ và Động học Dịch não tủy
Giấc ngủ không đơn thuần là trạng thái nghỉ ngơi mà là một quá trình sinh lý tích cực liên quan đến việc "làm sạch" não bộ. Phân tích gộp của Sabia và cộng sự (2021) trên Nature Communications với dữ liệu theo dõi 25 năm () đã xác lập mối quan hệ hình chữ U giữa thời lượng giấc ngủ và nguy cơ sa sút trí tuệ. Nguy cơ tăng cao ở nhóm ngủ giờ (HR = 1.30, 95% CI: 1.11–1.52).
Tuy nhiên, yếu tố quyết định không chỉ là thời lượng mà là vi cấu trúc giấc ngủ. Phát hiện về hệ thống Glymphatic (Glymphatic System) đã cách mạng hóa hiểu biết về cơ chế này. Trong giai đoạn ngủ sâu (NREM), các kênh nước aquaporin-4 mở rộng, cho phép dịch não tủy (CSF) thâm nhập sâu vào nhu mô não để rửa trôi Beta-amyloid và protein Tau. Sự gián đoạn giấc ngủ làm suy giảm hiệu suất của quá trình này, dẫn đến tích tụ độc tố thần kinh.
4. Bàn luận: Tương tác đa chiều và Phản biện khoa học
Dữ liệu tổng hợp cho thấy một mối quan hệ hai chiều (bidirectional relationship) phức tạp:
- Dinh dưỡng tác động lên Giấc ngủ: Chế độ ăn nhiều đường và carbohydrate tinh chế làm giảm thời lượng giấc ngủ sóng chậm (SWS) và tăng số lần thức giấc trong đêm thông qua cơ chế kháng insulin và biến động đường huyết.
- Giấc ngủ tác động lên Dinh dưỡng: Thiếu ngủ gây rối loạn hormone điều chỉnh sự thèm ăn (tăng Ghrelin, giảm Leptin), thúc đẩy hành vi tìm kiếm thực phẩm giàu năng lượng, tạo nên một vòng xoắn bệnh lý.
Hạn chế phương pháp luận: Cần thẳng thắn nhìn nhận rằng đa số các nghiên cứu (như Morris et al., 2015; Li et al., 2023) là nghiên cứu quan sát. Do đó, vấn đề "nhân quả ngược" (reverse causality) – liệu bệnh lý thần kinh tiềm ẩn gây rối loạn giấc ngủ hay ngược lại – vẫn là một thách thức chưa được giải quyết triệt để. Ngoài ra, việc sử dụng các công cụ tự báo cáo (như PSQI hay FFQ) có thể dẫn đến sai số nhớ lại (recall bias).
5. Kết luận và Khuyến nghị
Sự suy giảm nhận thức là kết quả của sự tích lũy tổn thương qua nhiều thập kỷ. Dựa trên các bằng chứng mức độ cao, can thiệp đơn lẻ là không đủ. Các nhà thực hành lâm sàng và giáo dục cần xây dựng các phác đồ can thiệp đa mô thức: kết hợp chế độ ăn MIND, tối ưu hóa vệ sinh giấc ngủ để bảo vệ hệ thống Glymphatic, và kiểm soát các chỉ số viêm hệ thống. Các nghiên cứu tương lai cần tập trung vào thử nghiệm lâm sàng ngẫu nhiên (RCT) với các dấu ấn sinh học (biomarkers) khách quan hơn để khẳng định quan hệ nhân quả.
Tài liệu tham khảo
Livingston, G., Huntley, J., Sommerlad, A., Ames, D., Ballard, C., Banerjee, S., ... & Mukadam, N. (2020). Dementia prevention, intervention, and care: 2020 report of the Lancet Commission. The Lancet, 396(10248), 413-446. https://doi.org/10.1016/S0140-6736(20)30367-6
Morris, M. C., Tangney, C. C., Wang, Y., Sacks, F. M., Barnes, L. L., Bennett, D. A., & Aggarwal, N. T. (2015). MIND diet slows cognitive decline with aging. Alzheimer's & Dementia, 11(9), 1015–1022. https://doi.org/10.1016/j.jalz.2015.04.011
Nedergaard, M., & Goldman, S. A. (2020). Glymphatic failure as a final common pathway to dementia. Science, 370(6512), 50–56. https://doi.org/10.1126/science.abb8739
Sabia, S., Fayosse, A., Dumurgier, J., van Hees, V. T., Paquet, C., Sommerlad, A., ... & Singh-Manoux, A. (2021). Association of sleep duration in middle and old age with incidence of dementia. Nature Communications, 12(1), 2289. https://doi.org/10.1038/s41467-021-22354-2

